Instytucja nadzorująca:
Narodowe Centrum Nauki
Kierownik projektu:
dr hab. Hanna Piotrowska-Kempisty
Budżet:
837 786,00 PLN
Data rozpoczęcia:
20.09.2017
Czas trwania:
36 miesięcy
Numer umowy:
UMO-2016/23/D/NZ7/03954
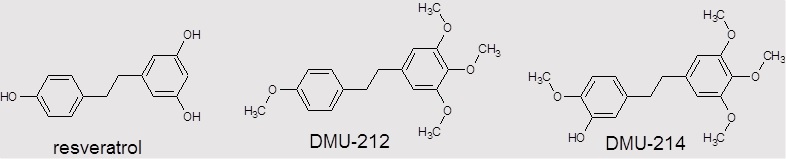
Nowotwory złośliwe, po chorobach układu krążenia, stanowią drugą najczęstszą przyczynę zgonów zarówno w Polsce, jak i na całym świecie. Rosnąca liczba zachorowań na nowotwory złośliwe oraz poważne działania niepożądane dostępnych obecnie strategii terapeutycznych wiążą się zarówno z wysokimi nakładami ekonomicznymi, jak i bardzo istotnymi kosztami społecznymi. Dlatego badania nad profilaktyką chorób nowotworowych oraz skuteczną, a zarazem bezpieczną dla pacjenta terapią stały się jednym z największych wyzwań współczesnych nauk biomedycznych. Enzymy z rodziny cytochromu P450 CYP1 tj. CYP1A1 oraz CYP1B1, które ulegają bardzo często nadekspresji w komórkach nowotworowych w porównaniu do otaczających je komórek prawidłowych, biorą udział w biotransformacji wielu pro-leków prowadzącej do powstania bardziej toksycznego metabolitu. Jego działanie jest również często ograniczone do środowiska guza. Wyniki badań autorów projektu wykazały, że metylowy analog resweratrolu DMU-212 (3,4,5,4’-tetrametoksystylben) o silnym działaniu przeciwnowotworowym ulega biotransformacji w komórkach raka jajnika do bardziej aktywnego metabolitu DMU-214 (3’-hydroksy-3,4,5,4’-tetrametoksystylbenu) o selektywnym działaniu, ograniczonym głównie do komórek nowotworowych.
Celem projektu jest ocena skuteczności przeciwnowotworowej DMU-214, metabolitu metylowego analogu resweratrolu DMU-212, w spersonalizowanej terapii raka jajnika. Badania zostaną przeprowadzone z wykorzystaniem komórek pochodzących od pacjentek z rakiem jajnika w modelach: in vitro hodowli komórkowej 3D oraz in vivo. Paklitaksel oraz karboplatyna, standardowo stosowane w leczeniu raka jajnika, indukują zróżnicowaną odpowiedź wśród pacjentek, a terapie celowane molekularnie są bardzo rzadko stosowane. W świetle tych danych niezwykle istotne jest opracowanie nowych modeli spersonalizowanego leczenia raka jajnika w oparciu o jego charakterystykę molekularną oraz genetyczną, która umożliwi przewidzieć odpowiedź pacjenta na zastosowaną terapię. Model 3D hodowli komórek pochodzących od pacjentek z rakiem jajnika ma na celu znacznie bardziej wiarygodne odwzorowanie warunków panujących w organizmie w stosunku do tradycyjnego, najczęściej stosowanego w eksperymentach in vitro „płaskiego” modelu 2D. Analizy in vitro zaproponowane w projekcie, oprócz normoksji, zostaną wykonane w stanie hipoksji (niedoboru tlenu), czyli w warunkach charakterystycznych dla środowiska guza. Jest to szczególnie ważny punkt projektu biorąc pod uwagę kluczową rolę obniżonego stężenia tlenu w tkance nowotworowej i jego wpływu na procesy metaboliczne komórki oraz skuteczność terapii.
Jak dotąd, według naszej najlepszej wiedzy, nie ma dostępnych danych w piśmiennictwie na temat działania przeciwnowotworowego metylowych analogów resweratrolu, w tym DMU-214, w stanie hipoksji. Hipoksja uznawana jest za negatywny czynnik w terapii nowotworów, w tym raka jajnika. Badania wstępne wnioskodawcy wykazały, zgodnie z oczekiwaniami, że działanie cytotoksyczne DMU-214 w komórkach raka jajnika było niższe w hipoksji (1% O2) w porównaniu do normoksji. Pomimo zaobserwowanego negatywnego wpływu obniżonego stężenia tlenu, działanie anty-proliferacyjne DMU-214 nadal jest dużo wyższe od karboplatyny stosowanej w terapii raka jajnika. Jak wiadomo, hipoksja odpowiada za oporność komórek nowotworowych na standardowe cytostatyki tj. karboplatyna czy paklitaksel. Dlatego też uzasadniona jest konieczność prowadzenia badań w zakresie mechanizmu działania potencjalnych chemioterapeutyków, w tym DMU-214, w zależności od stężenia tlenu. Ścieżki sygnałowe aktywowane w komórkach raka jajnika, które odpowiadają za zjawisko oporności indukowanej przez hipoksję nie są wystarczająco poznane. Planowane w projekcie analizy biochemiczne i molekularne, obejmujące analizy przesiewowe tj. mikromacierze ekspresyjne mogą przyczynić się do identyfikacji nowych markerów hipoksji oraz oporności komórek raka jajnika na chemioterapeutyki. W końcowym etapie realizacji projektu aktywność biologiczna badanego związku zostanie zweryfikowana w eksperymencie in vivo z wykorzystaniem myszy SCID - zdolnych do przyjęcia przeszczepu ludzkich nowotworów z uwagi brak limfocytów T i B. Wzrost guzów nowotworowych będzie monitorowany za pomocą zaawansowanego systemu obrazowania przyżyciowego.


